Dr. Marco V. Benavides Sánchez.
La inteligencia artificial (IA) está revolucionando el campo de la medicina, proporcionando herramientas avanzadas que mejoran la precisión diagnóstica y personalizan los tratamientos. Uno de los componentes esenciales de la IA en medicina es el entrenamiento de modelos, una tarea compleja y rigurosa que involucra varias etapas desde la definición del problema hasta la implementación del modelo en un entorno clínico.
Definición del Problema y Métricas de Evaluación
El primer paso en el entrenamiento de un modelo de IA es definir claramente el problema que se desea resolver. Por ejemplo, un objetivo podría ser la detección temprana de tumores en imágenes médicas o la predicción de enfermedades específicas basadas en datos clínicos. Esta definición no solo establece el enfoque del proyecto, sino que también determina las métricas de evaluación que se utilizarán para medir el rendimiento del modelo.
Las métricas de evaluación son fundamentales porque proporcionan una forma cuantitativa de evaluar qué tan bien está funcionando el modelo. Algunas métricas comunes incluyen la precisión, la sensibilidad (“recall”) y la especificidad. La precisión mide el porcentaje de predicciones correctas, la sensibilidad indica la capacidad del modelo para identificar correctamente las verdaderas positivas, y la especificidad refleja la capacidad del modelo para identificar correctamente las verdaderas negativas.
Recopilación y Preprocesamiento de Datos
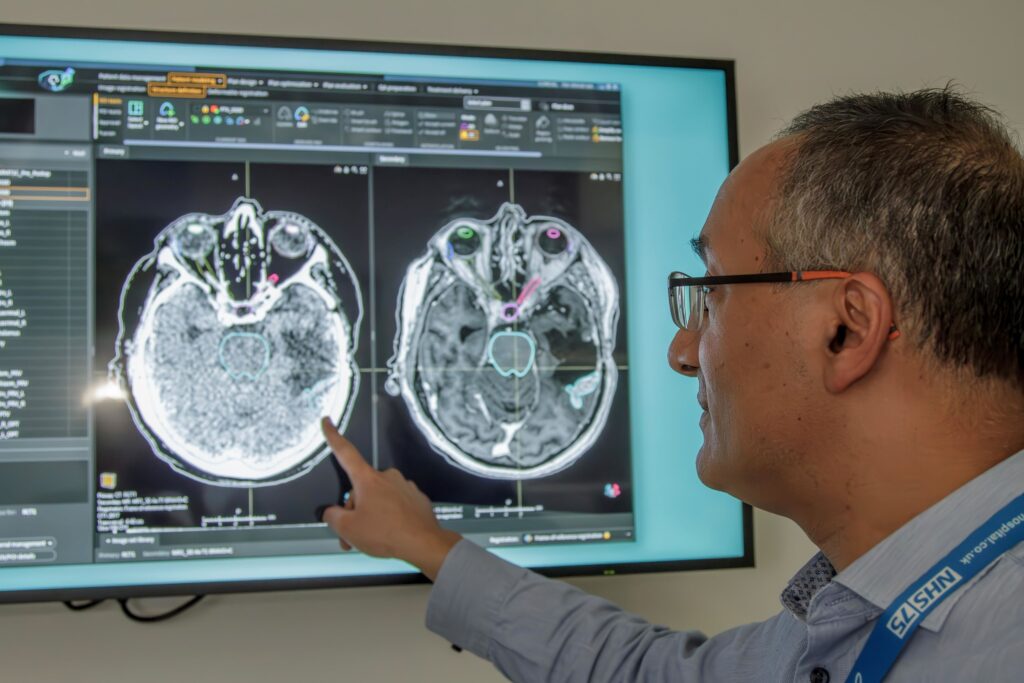
Una vez que se ha definido el problema y las métricas de evaluación, el siguiente paso es la recopilación y preprocesamiento de datos. Los datos son el combustible que alimenta cualquier modelo de IA, y en el campo de la medicina, estos datos pueden incluir imágenes de resonancias magnéticas, tomografías computarizadas, rayos X, historias clínicas electrónicas, entre otros.
El preprocesamiento de datos es una etapa crítica que implica la limpieza y normalización de los datos recopilados. Este proceso puede incluir la eliminación de ruido (datos irrelevantes o incorrectos), la corrección de errores y la conversión de los datos a un formato adecuado para el modelo. Por ejemplo, en el caso de las imágenes médicas, el preprocesamiento puede involucrar la segmentación de imágenes para destacar áreas de interés, la corrección de variaciones en el brillo y el contraste, y la reducción del tamaño de las imágenes para facilitar el procesamiento.
División de Datos y Elección de Modelo y Algoritmo
Una vez que los datos han sido preprocesados, se dividen en conjuntos de entrenamiento, validación y prueba. El conjunto de entrenamiento se utiliza para enseñar al modelo, el de validación para ajustar los hiperparámetros (valores externos al modelo que se establecen antes del entrenamiento) y el de prueba, para evaluar el rendimiento final del modelo.
La elección del modelo y el algoritmo adecuados es un paso esencial. En el caso del diagnóstico médico basado en imágenes, las redes neuronales convolucionales (CNN) son una opción común debido a su eficacia en el procesamiento de imágenes. Para otros tipos de datos, como historias clínicas, se pueden utilizar otros tipos de redes neuronales o algoritmos de aprendizaje automático, como los árboles de decisión o los modelos de bosques aleatorios (algoritmos de “machine learning” que combinan la salida de varios árboles de decisión para obtener un resultado único).

Entrenamiento y Optimización del Modelo
El entrenamiento del modelo implica el uso del conjunto de entrenamiento para ajustar los parámetros del modelo de manera que se minimice el error entre las predicciones y los valores reales. Este proceso se realiza de manera iterativa (repetir el proceso o una serie de pasos una y otra vez), utilizando algoritmos de optimización como el descenso de gradiente, que ajusta los pesos y sesgos del modelo para mejorar su rendimiento.
Durante el entrenamiento, es crucial monitorear el rendimiento del modelo en el conjunto de validación para evitar el sobreajuste (“overfitting”). El sobreajuste ocurre cuando el modelo se adapta demasiado a los datos de entrenamiento y no generaliza bien a datos nuevos. Para mitigar este problema, se pueden utilizar técnicas como la regularización, que penaliza la complejidad del modelo, o el “dropout”, que desactiva aleatoriamente neuronas durante el entrenamiento para mejorar la calidad del modelo.
Validación y Ajuste del Modelo
Después del entrenamiento inicial, se utiliza el conjunto de validación para ajustar los hiperparámetros del modelo, que son parámetros que determinan la estructura y el comportamiento del modelo, pero no se ajustan durante el entrenamiento. Ejemplos de hiperparámetros incluyen la tasa de aprendizaje, el número de capas en una red neuronal y el tamaño del lote de entrenamiento (conjunto de ejemplos de datos que se utilizan para entrenar un modelo).
La validación cruzada es una técnica común para ajustar hiperparámetros. En la validación cruzada, los datos de entrenamiento se dividen en varios subconjuntos, y el modelo se entrena múltiples veces utilizando diferentes combinaciones de estos subconjuntos. Esto permite evaluar el rendimiento del modelo de manera más robusta y seleccionar los mejores hiperparámetros.
Evaluación e Implementación en Entorno de Producción
Una vez que el modelo ha sido entrenado y ajustado, se evalúa su rendimiento en el conjunto de prueba, que contiene datos que el modelo no ha visto antes. Esta evaluación proporciona una medida de qué tan bien el modelo generaliza a datos nuevos y es una indicación de su desempeño en un entorno clínico real.
Si el rendimiento del modelo es satisfactorio, el siguiente paso es su implementación en un entorno de producción. Esto puede implicar la integración del modelo en sistemas de información hospitalarios, aplicaciones móviles o dispositivos médicos. Es crucial asegurar que el modelo sea interpretable y transparente para generar confianza en los profesionales de la salud y los pacientes. La interpretabilidad significa que los médicos deben poder entender y explicar las decisiones del modelo, mientras que la transparencia implica que el modelo debe proporcionar información sobre cómo se llegó a una decisión.
La Falta de Datos Etiquetados: Problemas y Soluciones
Un desafío significativo en el entrenamiento de modelos de IA en medicina es la falta de datos etiquetados. Los datos etiquetados son esenciales para supervisar el aprendizaje de los modelos, pero su obtención puede ser costosa y llevar mucho tiempo. A continuación, exploramos algunas estrategias para abordar este problema.
Los datos etiquetados son datos sin procesar, a los que se les ha asignado una o más etiquetas para añadirles contexto o significado. Estas etiquetas son como rótulos descriptivos que permiten que los modelos de « machine learning » comprendan y realicen predicciones más precisas. En otras palabras, las etiquetas sirven como objetivos para que el modelo aprenda a relacionar características específicas con resultados específicos.
Desde el inicio de cualquier proyecto de IA, es fundamental recopilar datos de alta calidad de manera rigurosa. Esto implica asegurarse de que los datos estén bien estructurados, documentados y vinculados a la información relevante del paciente. La recopilación cuidadosa de datos reduce la necesidad de etiquetar retrospectivamente y garantiza que los datos sean útiles para entrenar modelos precisos.
Transferencia de Aprendizaje (Transfer Learning)
La transferencia de aprendizaje es una técnica que permite aprovechar el conocimiento previamente adquirido por modelos entrenados en otras tareas. Por ejemplo, si se dispone de un modelo entrenado para detectar neumonía en radiografías de tórax, este modelo puede servir como punto de partida para desarrollar uno específico para detectar otras afecciones pulmonares. Transferir características aprendidas de un modelo preentrenado a uno nuevo acelera el proceso de entrenamiento y reduce la necesidad de grandes cantidades de datos etiquetados.
Etiquetación Semiautomática o Activa
En lugar de etiquetar manualmente todos los datos, se puede utilizar un enfoque semiautomático. Por ejemplo, un algoritmo puede sugerir etiquetas que luego serán revisadas y ajustadas por expertos. La etiquetación activa, por otro lado, implica etiquetar solo una pequeña parte inicial de los datos y luego seleccionar estratégicamente las muestras más informativas para etiquetar a medida que avanza el proceso. Esto reduce significativamente la carga de trabajo de los expertos humanos y maximiza la eficiencia del etiquetado.
Colaboración y Crowdsourcing
Las comunidades médicas y científicas pueden ser una valiosa fuente de colaboración para la etiquetación de datos. Involucrar a médicos, residentes o estudiantes en la tarea de etiquetar imágenes médicas puede acelerar el proceso y mejorar la calidad de las etiquetas. Además, las plataformas de « crowdsourcing » (aprovechar la inteligencia colectiva y la creatividad de la comunidad para resolver problemas, generar ideas o crear contenido), como Quirky, Kickstarter o Freelancer pueden ser útiles para obtener etiquetas de una audiencia amplia, aunque es crucial garantizar que los participantes tengan la capacitación adecuada para etiquetar datos médicos con precisión.
Conclusión
El entrenamiento de modelos de inteligencia artificial para el diagnóstico médico es un proceso complejo pero esencial que está cambiando radicalmente la medicina moderna. Desde la definición del problema y la recopilación de datos hasta la implementación en un entorno clínico, cada paso requiere una cuidadosa planificación y ejecución.
A pesar de los retos que se presentan en el proceso, como la falta de datos etiquetados, ya existen estrategias efectivas para superarlos y aprovechar al máximo el potencial de la IA en medicina. Al combinar avances tecnológicos con prácticas éticas y colaborativas, es posible mejorar significativamente la atención médica y ofrecer diagnósticos más precisos y personalizados a los pacientes.
Referencias:
1. Inteligencia Artificial en la Medicina | IBM.
2. Inteligencia artificial en medicina para salvar vidas – IAT.
3. Inteligencia Artificial en Medicina: Innovaciones y Aplicaciones.
4. Nuevo modelo de IA para el diagnóstico de enfermedades – ConSalud.es.
5. La inteligencia artificial en el diagnóstico médico – DATABOT.
ArtificialIntelligence #Medicine #Surgery #Medmultilingua


Deja un comentario